Abstracts Publicaciones 2021
Quiénes somos
Instrucciones a autores
Responsabilidad autoría
Contacto
Portal Revistas U. de Chile
Daño hepático crónico como manifestación de pericarditis constrictiva. Reporte de un caso
Constrictive pericarditis (CP) is an uncommon condition which clinical presentation becomes very unspecific, making its diagnosis a hard challenge. It has multiple and varied causes, all of them determine pericardium inflammation and progressive fibrosis that restricts heart filling and develops diastolic dysfunction, expressing mainly as right heart failure. Symptoms of this last condition allow posing different diagnosis as they can appear in many other diseases, including chronic liver disease as happens in the following clinical case. A 27 year-old male patient with a history of progressive edema on his extremities, increased abdominal volume, a 3-month body weight loss, and dyspnea; is firstly diagnosed as CLD after medical evaluation. However, etiological studies for CLD appear negative and the patient does not respond to general approaches, motivating his hospitalization for further studies. Cardiologic tests reveal pulmonary hypertension, which is studied by MRI showing a thickened pericardium suggesting constriction that is confirmed by cardiac catheterization. The patient undergoes surgery without incidents and a favorable post-operatory period, being completely asymptomatic 3 months later. This clinical case reflects how difficult can become diagnosing CP; as well as presenting the right way to study these patients in order to confirm this alternative diagnosis, the treatment of choice, and the excellent results that surgery can achieve. Finally, CP is a rare condition that must be included within differential diagnosis of patients with clinical manifestations of RHF.
Rev Hosp Clin Univ Chile 2015; 26(4): 336-42.
Héctor Ugalde P., María Ignacia Sanhueza F., María Cecilia Yubini L., Sebastián Rozas A., Stefanie Mundnich B., Mauricio Cereceda B., Cristóbal Ramos G.
La pericarditis constrictiva crónica (PC) es el estado final de una enfermedad inflamatoria que afecta al pericardio(1). Suele ser una enfermedad irreversible y lentamente progresiva, caracterizada por inflamación y fibrosis del pericardio, lo que dificulta el llenado cardíaco y finalmente conduce a una falla diastólica(2,3). Es una patología poco frecuente que se presenta en promedio a los 56 años y es más común en hombres (3:1)(4). Dentro de sus múltiples causas, las más frecuentes son idiopática, postcirugía cardíaca y actínica(4-6).
El cuadro clínico consiste principalmente en insuficiencia cardiaca derecha (edema pretibial, hepatomegalia, ascitis) sin o con pocos signos de insuficiencia cardiaca izquierda (disnea, fatiga)(1,2). Por eso, el signo clave es la ingurgitación yugular(1,2). En el examen físico se puede encontrar además un colapso “Y” profundo, knock pericárdico, signo de Kussmaul y/o pulso paradójico(1-3). Debido a lo inespecífico que resulta la sintomatología, para el diagnóstico es fundamental una alta sospecha clínica junto a un estudio exhaustivo con exámenes complementarios(1,2,7).
A continuación se presenta el caso de un hombre de 27 años en quien la PC simuló un cuadro de daño hepático crónico (DHC). El caso demuestra el desafío diagnóstico que puede representar la PC, ya que clínicamente sus síntomas pueden ser interpretados como distintas patologías.
CASO CLÍNICO
Paciente de sexo masculino de 27 años de edad, sin antecedentes mórbidos previos. Su historia comienza 6 meses previos al ingreso a nuestro Hospital, con edema de extremidades lentamente progresivo, a lo cual se agrega aumento de volumen abdominal y pérdida de peso con apetito conservado desde hace 3 meses, alcanzando 10 kg de baja de peso al ingreso. A esto se agrega disnea de esfuerzos moderados. Por todo esto consulta médico 2 meses atrás, efectuándose estudio consistente en hemograma (normal), función renal normal, pruebas hepáticas (alteradas, con GGT de 250 U/L, fosfatasas alcalinas y transaminasas normales, tiempo de protrombina de 60% con INR de 1.5). Se solicita ante esto ecotomografía abdominal que muestra hepatomegalia difusa y líquido libre peritoneal abundante, marcadores virales (VIH, VHC) y pruebas inmunológicas (ANA, ENA, ANCA, anticardiolipinas), resultando todo negativo. Se plantea el diagnóstico de DHC de etiología desconocida, iniciándose medidas generales. Pese a esto la sintomatología progresa y se agrega fatigabilidad por lo que es referido al Servicio de Gastroenterología de nuestro Hospital para mayor estudio y definir la mejor opción terapéutica.
Al examen físico de ingreso destaca hemodinamia normal (FC: 80, PA: 120/70), yugulares ingurgitadas, ascitis y marcado edema de extremidades inferiores.
Ingresa con el diagnóstico de DHC en estudio. Se solicita nueva ecografía abdominal y endoscopía digestiva alta. La primera muestra hepatomegalia difusa con cambios morfológicos compatibles con DHC y signos de hipertensión portal, la segunda evidencia varices esofágicas de grado leve. Con estos datos y la exploración física, el gastroenterólogo solicita electrocardiograma que evidencia disminución de voltajes en precordiales y alteraciones inespecíficas de repolarización y ecocardiograma que muestra un ventrículo izquierdo y derecho normales, leve dilatación biauricular, sin alteraciones valvulares, hipertensión pulmonar moderada a severa (sistólica de 65mmhg) y ausencia de shunt izquierda-derecha.
Ante estos resultados se solicita evaluación cardiológica. Este plantea el diagnóstico de probable hipertensión pulmonar primaria, sugiriendo estudio de imágenes primero con angioTac de tórax, el cual es normal, seguido de ecocardiograma transesofágico a fin de determinar presencia o ausencia de shunt. Este descarta esta posibilidad por lo que se completa el estudio con resonancia nuclear magnética de corazón (RNM), la cual muestra ascitis, dilatación de vena cava inferior (Figura 1), engrosamiento pericárdico con dilatación biauricular y configuración tubular de los ventrículos (Figura 2), planteándose el diagnóstico de pericarditis constrictiva. Ante estos hallazgos se define realizar sondeo cardiaco, el cual muestra hipertensión pulmonar moderada, con aumento de presiones intracavitarias, igualamiento de presiones finales diastólicas de ambos ventrículos e imagen de raíz cuadrada en el registro, hechos sugerentes de constricción pericárdica (Figura 3 y Tabla 1).
Figura 1. RMN cardiaca
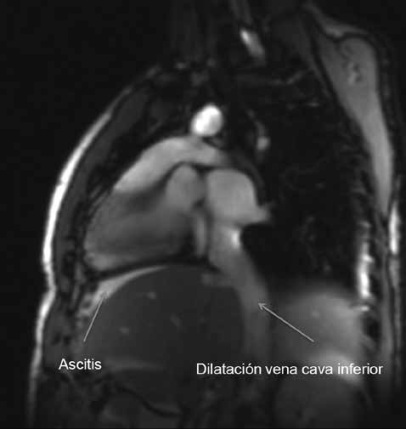
Figura 2. RMN cardiaca
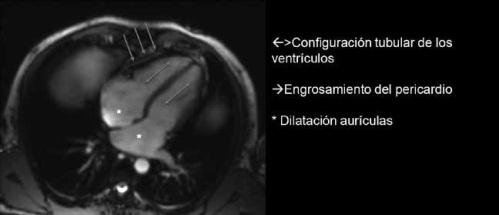
Tabla 1. Sondeo cardiaco

Figura 3. Sondeo cardiaco:
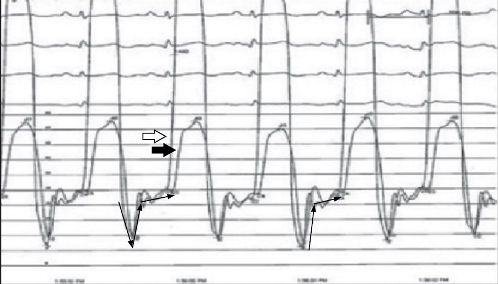
- Registro simultáneo en presiones en VI ( ) - VD (
) - VD ( )
)
- Ascenso rápido en presión diástole ( )
)
- Poca variación en resto diástole (Plateau) ( )
)
- Imagen de raíz cuadrada ( )
)
Confirmado el diagnóstico de pericarditis constrictiva, se define resolución quirúrgica. Esto se efectúa 3 días después, realizándose pericardiectomía
de pared lateral, anterior e inferior. Se conserva la pared posterior pues en el ecocardiograma transesofágico intrapabellón no se observa engrosado. La cirugía se realiza a corazón latiendo sin necesidad de circulación extracorpórea, controlando el resultado con ecocardiograma intraesofágico, el cual muestra una mejoría notoria del llene y la movilidad del ventrículo derecho. La PVC baja de 24 a 12. Posteriormente, el paciente evolucionó favorablemente sin complicaciones y fue dado de alta a la semana de la cirugía, solo con medidas generales. La biopsia arrojó inflamación crónica inespecífica. A los 3 meses el paciente presenta resolución completa de sus síntomas, sin edema ni ascitis.
DISCUSIÓN
El caso expuesto corresponde a una presentación atípica de PC crónica. Esta enfermedad se debe a inflamación y fibrosis del pericardio visceral y/o parietal de más de tres meses(8) que puede evolucionar con engrosamiento y calcificaciones pericárdicas(1). El grado de restricción que se produce del llenado diastólico determinará la intensidad de los síntomas, los cuales suelen ser inicialmente leves con una evolución progresiva en meses y años. Los síntomas y signos son variados, siendo los más frecuentes aquellos que reflejan insuficiencia cardiaca derecha(1) como ingurgitación yugular, hepatomegalia y edema periférico(4,9), los que se presentaron inicialmente en nuestro paciente. Al examen físico, el característico knock pericárdico se ausculta en una baja proporción de pacientes(4) y puede confundirse un ruido S3. Otros signos como el signo de Kussmaul’s y de Friedreich’s pueden estar presentes. Ninguno de ellos es especifico de PC(10). En el caso descrito, además se agregan signos de DHC secundario a congestión venosa, como ascitis clara, aumentando la dificultad diagnóstica.
Debido a lo anterior, el cuadro clínico de la PC se puede confundir con múltiples patologías. Entre ellas, destaca el tromboembolismo pulmonar, enfermedades pulmonares obstructivas o intersticiales, miocardiopatía restrictiva e incluso enfermedades gastrointestinales como DHC hasta cirrosis(8). Por eso, la sospecha clínica del médico es fundamental para dirigir adecuadamente el estudio del paciente. En nuestro caso el abordaje inicial se dirigió al estudio del DHC y ante la falta de diagnóstico específico y la falla de las medidas terapéuticas iniciales, es que fue referido a nuestro Hospital. Allí al gastroenterólogo le llamó la atención la marcada ingurgitación yugular y solicitó estudio cardiológico básico y desde allí cambió el planteamiento diagnóstico.
Frente a la sospecha de PC se deben realizar una serie de exámenes complementarios que incluyen electrocardiograma -el cual puede mostrar disminución de voltajes y alteraciones de onda t y segmento st no específicas(11), como así ocurrió en nuestro paciente y radiografía de tórax (que puede mostrar calcificaciones a nivel pericárdico(11)- y específicamente, un ecocardiograma(3,4,11), el cual se considera el examen de primera elección en cualquier caso que se sospeche una enfermedad pericárdica(12). Con él podemos identificar el aumento característico de la interdependencia ventricular con la respiración, detectar engrosamiento pericárdico, dilatación de cavidades y vena cava y al Doppler evidenciar llene diastólico rápido y restrictivo y además hacer diagnóstico diferencial(13) con otras causas de falla ventricular derecha. En el caso descrito, el ecocardiograma mostró hipertensión pulmonar y leve dilatación biauricular sin otros signos que hicieran sospechar enfermedad pericárdica, pero cabe la consideración que este estudio fue hecho con la sospecha de DHC y no fue buscado dirigidamente un problema al pericardio, pues hasta el momento no se había sospechado. Otros estudios útiles en el diagnóstico son la TAC cardiaca y la RMN cardiaca(11). El primero de ellos muy útil en evaluar la calcificación pericárdica, pero no tan adecuado para la evaluación funcional como el ecocardiograma o la resonancia nuclear magnética cardiaca que permite una evaluación morfológica, evaluar las consecuencias fisiológicas de la enfermedad pericárdica, diferenciar entre pericarditis constrictiva de miocardiopatía restrictiva, con la ventaja de no utilizar radiación ionizante(14-16). En el caso descrito la RMN mostró el engrosamiento pericárdico, dilatación de cavidades y signos de hipertensión venocapilar, lo que hizo plantear en forma inmediata el diagnóstico de PC. Eventualmente se puede realizar un cateterismo cardíaco(3,4,11) en busca de signos claros de constricción como aumento de la presión atrial, ecualización de las presiones de las cámaras cardíacas al final de la diástole, signo de la “raíz cuadrada” o “dip & plateu”, y cambios en la variación del llenado y de la presión sistólica de los ventrículos con la respiración(7), hallazgos evidenciados en forma clara en nuestro paciente. El tratamiento curativo para esta enfermedad es la pericardiectomía parcial o total (de preferencia total)(11,17). Esta operación se asocia a una mortalidad a 30 días que varía entre un 5 y 15%(4,6,9,17), la cual aumenta en pacientes con PC actínica y con capacidad funcional (CF) III-IV(6,9). Por otra parte, en estudios a largo plazo la sobrevida es buena con porcentajes a 5-7 años de evolución que oscilan cercanos al 80%(4,6,9,17), donde solo el 25 ± 5% se mantiene sintomático con CF III-IV(4) . En esta etapa factores de mal pronóstico son PC actínica, alteración de la función renal, aumento de la presión sistólica de la arteria pulmonar, disfunción sistólica del ventrículo izquierdo, hiponatremia, edad avanzada, hiperbilirrubinemia, fibrilación auricular y factores relacionados a la técnica quirúrgica (pericardiectomía parcial)(6,17). También algunos autores consideran un elemento ominoso la calcificación pericárdica extensa, pero las publicaciones respecto al tema son contradictorias.
En conclusión, si bien el cuadro clínico de la PC y su manejo están bastante descritos por la literatura, su diagnóstico continúa siendo un desafío, principalmente por una falta de sospecha, debido a que es una enfermedad rara de observar en la práctica clínica. Es por eso que esta enfermedad no se busca dirigidamente y se confunde con otras patologías más comunes. En este caso, la dificultad se encontraba en reconocer a la PC como una posible etiología de DHC secundario a la congestión hepática crónica. Por lo tanto, a pesar de que la PC es una enfermedad infrecuente, se recomienda su sospecha siempre que exista un cuadro clínico compatible con insuficiencia cardíaca derecha, ya que es una enfermedad con tratamiento curativo y buenos resultados en el largo plazo.
REFERENCIAS
1. LeWinter M, Hopkins W. Cap. 71: Pericardial Diseases. En: Libby P, Bonow R, Mann D, Zipes D. Braunwald’s Heart Disease, 10th ed. Saunders Elsevier; Philadelphia, 2015: 1646-50.
2. Sagristà-Sauleda, J. Síndromes de constricción cardíaca. Rev Esp Cardiol 2008;61(Supl. 2):33-40.
3. Syed F, Schaff H, Oh J. Constrictive pericarditis [mdash] a curable diastolic heart failure. Nature Reviews Cardiology 2014;11:530-44.
4. Ling L, Oh J, Schaff H, Danielson G, Mahoney D, Seward J et al. Constrictive pericarditis in the modern era evolving clinical spectrum and impact on outcome after pericardiectomy. Circulation 1999;100:1380-6.
5. Cameron J, Oesterle S, Baldwin J, Hancock E. The etiologic spectrum of constrictive pericarditis. Am Heart J 1987;113:354-60.
6. Bertog S, Thambidorai S, Parakh K, Schoenhagen P, Ozduran V, Houghtaling P et al. Constrictive pericarditis: etiology and cause-specific survival after pericardiectomy. J Am Coll Cardiol 2004;43:1445-52.
7. Khandaker M, Espinosa R, Nishimura R, Sinak L, Hayes S, Melduni R et al. Pericardial disease: diagnosis and management. Mayo Clinic Proceedings 2010;85:572-93.
8. Maisch B, Seferovic P, Ristic A, Rienmüller R, Adler Y, Tomkowski W et al. Grupo de Trabajo para el Diagnóstico y Tratamiento de las Enfermedades del Pericardio de la Sociedad Europea de Cardiología. Guía de Práctica Clínica para el diagnóstico y tratamiento de las enfermedades del pericardio. Versión resumida. Rev Esp Cardiol 2004;57:1090-114.
9. Peset A, Martí V, Cardona M, Montiel J, Guindo J, de Rozas J. Resultados de la pericardiectomía por pericarditis constrictiva crónica. Revi Esp Cardiol 2007;60:1097-101.
10. Myers R, Spodick D. Constrictive pericarditis: clinical and pathophysiologic characteristics. Am Heart J 1999;138:219–32.
11. Adler Y, Charron P, Imazio M, Badano L, Baron G, Bogaert J et al . Guidelines for the diagnosis and management of pericardial diseases.The Task Force for the Diagnosis and Management of Pericardial Diseases of
the European Society of Cardiology (ESC). Endorsed by: The European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2015;36:2921-64.
12. Klein A, Abbara S, Agler D, Appleton C, Asher C, Hoit B et al. American Society of Echocardiography clinical recommendations for multimodality cardiovascular imaging of patients with pericardial disease: endorsed by the Societyfor Cardiovascular Magnetic Resonance and Society of Cardiovascular Computed Tomography. J Am Soc Echocardiogr 2013;26:965-1012.
13. Verhaert D, Ruvin G, Johnston D. The role of multimodality imaging in the management of pericardial disease. Circ Cardiovasc Imaging 2010;3:333-43.
14. Cosyns B, Plein S, Nihoyanopoulos P, Smiseth O, Achenbach S, Andrade M et al. On behalf of the European Association of Cardiovascular
Imaging (EACVI) and European Society of Cardiology Working Group (ESC WG) on Myocardial and Pericardial diseases. European Association of Cardiovascular Imaging (EACVI) position paper: multimodality imagingin pericardial disease. Eur Heart J Cardiovasc Imaging 2014;16:12–31.
15. Bogaert J, Francone M. Cardiovascular magnetic resonance in pericardial diseases. J Cardiovasc Magn Reson 2009;11:14.
16. Francone M, Dymarkowski S, Kalantzi M, Rademakers F, Bogaert J. Assessment of ventricular coupling with real-time cine MRI and it value to differentiate constrictive pericarditis from restrictive cardiomyopathy. Eur Radiol 2006;16:944–51.
17. Chowdhury U, Subramaniam G, Kumar A, Airan B, Singh R, Talwar S et al. Pericardiectomy for constrictive pericarditis: a clinical, echocardiographic, and hemodynamic evaluation of two surgical techniques. Ann Thorac Surg 2006;81:522-9.
Correspondencia:
 Dr. Héctor Ugalde Prieto
Dr. Héctor Ugalde Prieto
 Departamento Cardiología, HCUCH.
Departamento Cardiología, HCUCH.
 [email protected]
[email protected]
 562 2978 8355
562 2978 8355