Abstracts Publicaciones 2021
Quiénes somos
Instrucciones a autores
Responsabilidad autoría
Contacto
Portal Revistas U. de Chile
Estrategias de rehabilitación en paciente con ganglionopatía sensitiva asociada a síndrome
de Sjögren: reporte de un caso
RESUMEN
Introducción: Las ganglionopatías son trastornos infrecuentes que comprometen los cuerpos neuronales sensitivos en ganglios de raíz dorsal y ganglio trigeminal. Su etiología es heterogénea y su identificación permite tratamientos farmacológicos específicos; sin embargo, la evidencia sobre rehabilitación es escasa. Objetivo: Describir la evolución clínica y las estrategias de rehabilitación intrahospitalaria en una paciente con ganglionopatía secundaria a síndrome de Sjögren. Métodos: Reporte de caso y revisión narrativa. En paralelo al estudio etiológico y al tratamiento inmunomodulador, la paciente realizó un programa intensivo de rehabilitación intrahospitalaria en Medicina Física y Rehabilitación durante 24 días: neurokinesiología y terapia ocupacional (2 sesiones diarias de 60 min) y fonoaudiología (3–4 sesiones/semana de 60 min). Resultados: Hubo mejoría funcional medida con índice de Barthel, de 35 (dependencia grave) a 65 (dependencia moderada), con mayores avances en alimentación, arreglo personal y vestuario. La velocidad de marcha en 10 m aumentó de 0,48 a 0,62 m/s. Se redujo el territorio de hipoestesia térmico-táctil y apalestesia, con mejoría parcial de la sensibilidad oral. Al egreso: Berg 14/56 y SARA 13/40 como línea basal de seguimiento. Conclusiones: La rehabilitación intrahospitalaria integral puede asociarse a mejoras clínicamente relevantes en independencia funcional y marcha en ganglionopatía sensitiva; se requiere mayor evidencia.
Palabras clave: ganglionopatía sensitiva, neuronopatía sensitiva, síndrome de Sjögren, rehabilitación
SUMMARY
Introduction: Sensory ganglionopathies are uncommon disorders affecting sensory neuronal cell bodies in the dorsal root ganglia and trigeminal ganglion. Etiologies are heterogeneous, and identifying the cause may enable targeted pharmacologic treatment; however, evidence on rehabilitation is limited. Objective: To describe the clinical course and inpatient rehabilitation strategies in a patient with sensory ganglionopathy secondary to Sjögren’s syndrome. Methods: Case report and narrative review. Alongside etiologic workup and immunomodulatory therapy, the patient completed a 24-day intensive inpatient program in Physical Medicine and Rehabilitation: neuro-physiotherapy and occupational therapy (two 60-min sessions daily) and speech-language therapy (3-4 weekly 60-min sessions). Results: Functional improvement was documented with the Barthel Index, increasing from 35 (severe dependence) to 65 (moderate dependence), with greatest gains in feeding, personal grooming, and dressing. Ten-meter walking speed increased from 0.48 to 0.62 m/s. Sensory findings improved, with reduced thermal–tactile hypoesthesia and pallesthesia deficits and partial recovery of oral sensation. At discharge, Berg Balance Scale was 14/56 and SARA 13/40 as follow-up baseline measures. Conclusions: Comprehensive inpatient rehabilitation may be associated with clinically meaningful gains in functional independence and gait in sensory ganglionopathy; further evidence is needed to define the most effective strategies.
Keywords: sensory ganglionopathy, sensory neuronopathy, Sjögren’s syndrome, rehabilitation
Rev Hosp Clín Univ Chile 2026; 37: 26 - 35. DOI: 10.5354/2735-7996.2026.80928
Javier Pizarro S., Andrea Gallardo G., Jaime Vallejos G.
Las ganglionopatías o neuronopatías sensitivas constituyen una subcategoría de neuropatías periféricas(1) caracterizadas por el compromiso de los ganglios de la raíz dorsal y del ganglio trigeminal(2). Su presentación clínica suele ser exclusivamente sensitiva, sin déficit motor y puede abarcar territorios faciales, cuero cabelludo, mucosa oral, tronco y segmentos proximales de extremidades(3). Con frecuencia predominan las fibras gruesas, con pérdida de tacto, vibración y propiocepción, postura pseudoatetósica y Romberg positivo. El compromiso de fibras finas es variable(2).
Su relevancia clínica radica en que pueden ser manifestación inicial de una enfermedad sistémica subyacente. Las etiologías se agrupan en causas paraneoplásicas, infecciosas, autoinmunes, tóxicas e idiopáticas(2). En el síndrome de Sjögren, entre 5–15% de los pacientes presenta polineuropatías. De ellas, aproximadamente 40% corresponde a compromiso sensitivo de fibras gruesas; 20%, a fibras delgadas y el resto, a otros patrones (mononeuropatía múltiple, neuropatías craneales, autonómicas, entre otras)(2,3).
El diagnóstico precoz es fundamental e integra clínica y estudios inmunológicos (ANA, anti-Ro y anti-La), además de pesquisa de cáncer oculto y biopsia de tumores sospechosos o de parótidas en casos seronegativos de Sjögren(1,3). La neuroconducción sensitiva suele mostrar disminución de amplitud o ausencia de potenciales de acción sensitivos (SNAP), con conducción motora y electromiografía de aguja normales(4). La resonancia magnética puede evidenciar edema con hiperintensidad T2 o realce en ganglios de raíz dorsal, y/o degeneración de columnas posteriores medulares(2).
El tratamiento incluye glucocorticoides, inmunosupresores, plasmaféresis, inmunoglobulina o rituximab. En presencia de neoplasia, el tratamiento oncológico no asegura remisión, aunque podría limitar la progresión del daño neuronal(2). En rehabilitación, la evidencia específica es escasa: gran parte se extrapola desde estrategias usadas en ataxia cerebelosa y neurorrehabilitación(5), posiblemente por la baja frecuencia y el amplio espectro funcional pese a diagnósticos similares.
A continuación, se presenta el caso de una paciente con ganglionopatía secundaria a síndrome de Sjögren, describiendo rehabilitación intrahospitalaria, estrategias y evolución funcional. Se cuenta con consentimiento informado y autorización explícita para uso de imágenes del proceso.
DESCRIPCIÓN DEL CASO
Paciente femenina de 51 años con antecedentes de síndrome de Sjögren, hipotiroidismo e hipertensión arterial esencial. Inicia con dolor plantar bilateral y parestesias en extremidades inferiores, con progresión a extremidades superiores e hipoestesia facial perioral. Se agrega deterioro de la marcha e incapacidad para mantener bipedestación independiente. Al examen físico presenta hipoestesia facial y reflejo corneal bilateral disminuido; en extremidades, fuerza global M4+, arreflexia e hipotonía. En sensibilidad destaca hipoestesia e hipoalgesia de predominio distal, hipopalestesia en extremidades superiores y alteración severa de sensibilidad profunda en extremidades inferiores (abatiestesia y apalestesia). Se observa dismetría en cuatro extremidades. En control axial mantiene buen control de tronco estático y dinámico; en bipedestación, Romberg positivo. Logra marcha inestable con andador y asistencia de una persona.
Se hospitaliza con diagnóstico de ataxia sensitiva de probable origen autoinmune. El estudio etiológico evidencia anti-Ro positivo, ANA patrón granular fino y ANCA patrón atípico. La resonancia magnética de médula muestra polirradiculitis y compromiso de cordones posteriores, interpretados como ganglionopatía con degeneración axonal retrógrada. El estudio electrodiagnóstico demuestra compromiso sensitivo axonal multisegmentario con velocidades y amplitudes motoras preservadas. En conjunto, los hallazgos son compatibles con ganglionopatía sensitiva secundaria a síndrome de Sjögren.
Se inicia tratamiento con metilprednisolona en bolos (3 dosis) y luego inmunoglobulina intravenosa (5 dosis) sin mejoría clínica documentada, por lo que se realiza plasmaféresis (5 sesiones). Posteriormente se consigna mejoría clínica que facilita participación en terapia e ingreso a Medicina Física y Rehabilitación. No obstante, no se dispone de mediciones funcionales estandarizadas inmediatamente postplasmaféresis para cuantificar su contribución relativa. Continúa con prednisona en descenso progresivo asociada a micofenolato.
Tras completar el estudio y estabilizarse clínicamente, ingresa a un programa intensivo de rehabilitación intrahospitalaria. Los objetivos principales fueron maximizar independencia en actividades de la vida diaria (con independencia o baja asistencia) y lograr marcha intradomiciliaria con ayuda técnica. Se otorga alta a los 45 días con continuidad de rehabilitación y controles ambulatorios. La Figura 1 resume los hitos del proceso.

MÉTODOS: INTERVENCIONES DE REHABILITACIÓN
Se llevó a cabo una intervención interdisciplinaria orientada a: (I) compensación sensorial y propioceptiva, (II) entrenamiento de equilibrio y marcha, (III) optimización de AVD (autocuidado, transferencias, movilidad) y (IV) manejo de alteración de la deglución y sensibilidad oral.
Componentes por objetivo
• Equilibrio y control axial: entrenamiento en sedente y bípedo con apoyo progresivo, facilitación del control postural, tareas con retroalimentación visual (espejos) y transición a tareas duales cuando la seguridad lo permitió.
• Marcha: práctica repetida de marcha en pasillo con ayuda técnica, énfasis en control visual del apoyo, reducción progresiva del nivel de asistencia y educación en prevención de caídas.
• AVD: práctica de aseo y vestuario con adaptación del entorno, estrategias compensatorias y uso de prendas compresivas para aumentar input táctil profundo durante tareas finas.
• Sensibilidad: estimulación táctil y térmica con materiales de distintas texturas en manos/pies; estimulación vibratoria y propioceptiva (diapasón, pruebas de posición) y estimulación quimiotermotáctil intraoral según tolerancia.
Progresión y criterios de avance
La progresión se basó en: (I) tolerancia al esfuerzo sin eventos adversos, (II) disminución del nivel de asistencia requerido, (III) estabilidad postural y seguridad (disminución del riesgo de caídas) y (IV) capacidad de incorporar mayor complejidad en las actividades (p. ej., tareas duales, mayor distancia de marcha o menor apoyo).
Dosis terapéutica: Por el carácter retrospectivo del reporte, no se dispone de registro estandarizado y sistemático de RPE o minutos efectivos en cada sesión. No obstante, la dosis terapéutica se documenta en términos de frecuencia y duración de sesiones: neurokinesiología (2 sesiones diarias de 60 min), terapia ocupacional (2 sesiones diarias de 60 min) y fonoaudiología (3-4 sesiones/semana de 60 min). Además, se realizaron pausas según tolerancia clínica y seguridad.
Prendas compresivas: Se utilizaron prendas compresivas en extremidades superiores (mangas/ guantes compresivos) durante sesiones seleccionadas de terapia y actividades de AVD con el objetivo de aumentar aferencia táctil profunda. La presión de las medias compresivas fue de 18 mmHg.
Velocidad de marcha en 10 metros (10MWT): La velocidad se registró a velocidad confortable en un trayecto recto, utilizando un tramo central cronometrado y considerando espacio de aceleración y desaceleración para evitar sesgo por partida y detención. Se documentó la ayuda técnica y el nivel de asistencia(14,15).
ESTRATEGIAS DE REHABILITACIÓN UTILIZADAS Y SU FUNDAMENTO
Para cumplir los objetivos de rehabilitación se utilizaron las siguientes técnicas:
1. Estrategias cognitivas, utilizando la concentración para la realización de actividades motoras que previamente eran automáticas. Aquí se incluye, también, el uso de retroalimentación visual por medio del uso de espejos.
Al no tener la retroalimentación de los sistemas sensoriales internos (discriminación táctil, propiocepción, reconocimiento de formas y vibración), la paciente se valía del uso de estímulos visuales externos, en forma directa o por medio del uso de espejos. Esto requiere un mayor uso de la atención en la realización de tareas y, por lo tanto, mayor demanda cognitiva(6). Posteriormente, conforme se fue alcanzando la recuperación sensorial, se pudieron aplicar tareas duales, las que permiten disminuir su concentración en la tarea principal. Si bien la evidencia sobre el beneficio del uso de tareas duales en ataxias cerebelosas es contradictoria(7), es necesario su entrenamiento ya que la mayor parte de las actividades de la vida diaria demandan atención dividida.
2. Uso de prendas compresivas y pesas en las extremidades para entregar estímulo táctil profundo y, de esta manera, dar información propioceptiva que mejore la organización del movimiento.
En la literatura se ha descrito beneficio del uso de pesas en extremidades para la dismetría de pacientes con ataxia cerebelosa; sin embargo, no se ha estudiado su uso en pacientes con ataxia sensitiva(8). No obstante, durante el período de rehabilitación la paciente refirió un mejor desempeño con el uso de las prendas compresivas y las pesas en sus extremidades (Figuras 2 y 3). Para el caso de las prendas compresivas, su uso se tradujo en mejorías funcionales en la realización de actividades, como la alimentación y aseo personal, expresadas en el índice de Barthel, como se detallará a continuación.

Figura 2. Uso de prendas compresivas en extremidades superiores. Estrategia orientada a aumentar
la aferencia táctil profunda y facilitar la organización del movimiento durante tareas de AVD (p. ej., aseo personal y vestuario),
complementando la retroalimentación visual en actividades finas.
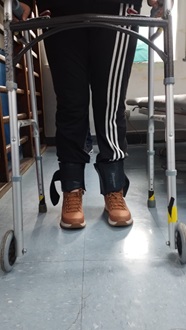
Figura 3. Uso de pesas de tobillo en extremidades inferiores. Implementadas durante tareas seleccionadas
de bipedestación y marcha para modular la dismetría y favorecer estabilidad, con monitorización de seguridad y
]tolerancia (pausas según fatiga).
3. Estímulos sensitivos en manos, pies y cavidad oral. Se utilizaron objetos de diferentes texturas (algodón, cepillos con cerdas de distintas durezas, alfombras texturizadas, entre otras) para someter a la paciente a estimulación táctil con el fin de reactivar progresivamente la función sensitiva de sus extremidades (Figuras 4 y 5). También, se dio estimulación quimiotermotáctil en cavidad oral, considerando la alteración derivada del compromiso de los ganglios trigeminales.

Figura 4. Estimulación táctil de extremidades inferiores. Ejemplos de estimulación con diferentes texturas
para favorecer recuperación/progresión sensitiva y mejorar
la seguridad durante la marcha mediante mayor información aferente.

Figura 5. Estimulación vibratoria de extremidades superiores. Uso de estimulación vibratoria/propioceptiva (p. ej., diapasón)
como complemento de reentrenamiento sensitivo y
apoyo a la función manual en AVD.
EVOLUCIÓN DE LOS DÉFICITS Y PRINCIPALES OUTCOMES FUNCIONALES
Ataxia
a. El control estático y dinámico de tronco progresa desde requerir asistencia de un evaluador hasta lograrlo de forma independiente.
b. En bípedo, alcanza el control estático con apoyo lateral, requiriendo mantener el input visual.
c. Logra avanzar desde una marcha con asistencia moderada a alta de un terapeuta a marcha independiente con andador de dos ruedas y supervisión externa.
Sensibilidad
a. Termalgesia: Se observa un aumento del área de sensibilidad táctil y térmica presente en sus extremidades. Al alta refiere sólo zonas de hipoestesia distal en ambos antebrazos.
b. Sensibilidad profunda: En relación con la batiestesia y palestesia, su mejoría se evidencia en mayor número de acierto con pruebas específicas de batidas en ortejos o uso de diapasón.
c. Sensibilidad oral: presenta mejoría en percepción de temperaturas y texturas intraorales, manteniendo territorio de hipoestesia en el paladar, tercio anterior de la lengua y región perioral.
d. Dolor: Durante la estadía hospitalaria la paciente no presentó dolor neuropático, por lo que no requirió tratamiento específico.
Outcomes funcionales
La Tabla 1 resume los principales cambios funcionales observados, cuyo detalle e interpretación se profundiza a continuación.

1. Índice de Barthel (0–100): Durante la rehabilitación intrahospitalaria, la paciente presentó una mejoría funcional significativa, con aumento del índice de Barthel desde 35/100 a 65/100 (+30 puntos), lo que representa una transición desde dependencia grave a dependencia moderada. El desglose por ítems sugiere que los principales avances se concentraron en actividades con impacto directo en la carga de cuidado: alcanzó independencia en alimentación, baño y arreglo personal, y mejoró en uso de inodoro y transferencias cama-silla, disminuyendo el nivel de asistencia requerido para AVD básicas. En movilidad, progresó desde un estado prácticamente inmóvil a una movilidad funcional en superficies planas con silla de ruedas a mayores distancias, mientras que las escaleras permanecieron imposibles y el vestuario continuó requiriendo ayuda parcial. En pacientes con patologías neurológicas como el ACV se ha propuesto una diferencia mínima clínicamente importante cercana a 9 puntos en Barthel 0–100(9), por lo que el cambio observado (+30) es consistente con una mejoría clínicamente relevante, aunque no existen puntos de corte específicos para ganglionopatía sensitiva. En un reporte de caso (n=1) no se realizaron análisis estadísticos; la interpretación se plantea en términos de significado funcional.
2. Escala de balance de BERG: la paciente obtuvo un puntaje de 14/56 puntos al egreso. El trastorno severo del balance no permitió plantear la realización segura de la prueba al inicio. Usualmente, pacientes en esta condición pueden puntuar, como máximo, 2 a 3 puntos. Esto es, sólo logran pasar del sedente al bípedo con uso de sus extremidades superiores (3 puntos) o lo logran con apoyo y luego de varios intentos (3 puntos). Por lo tanto, aunque el puntaje obtenido fue bajo, determinando un alto riesgo de caídas (menor a 45 puntos)(10), este valor constituye una mejoría per se respecto a la situación inicial y determina una medición basal para el seguimiento del trastorno del balance.
3. Escala para la evaluación y calificación de la ataxia (SARA): La paciente obtuvo un puntaje de 13/40, con el desglose que demuestra a continuación: marcha 6 puntos, bipedestación 3 puntos, sedente 3 puntos, alteración del habla 0 puntos, persecución de los dedos 1,5 puntos (derecho 1 e izquierdo 2), test dedo-nariz 1,5 puntos (derecho 1 e izquierdo 2), movimiento alternado de manos 0 puntos y test talón-espina 1 punto.
El puntaje obtenido en SARA fue principalmente determinado por la dificultad severa en la marcha y en la bipedestación, logrando una deambulación menor a 10 metros y requiriendo la asistencia de un terapeuta para lograrlo. El resto de los ítems de la escala presentaron puntaje normal o con una leve alteración y aunque no existen puntajes de corte para determinar la severidad de la ataxia, el puntaje global podría ser interpretado como un valor de afectación al menos moderado(11). En virtud de hacer visibles de forma más notoria los cambios en esta escala, se determinó no volver a medirla, sino hasta el período ambulatorio, por lo que no se cuenta con un registro pre y post rehabilitación intrahospitalaria. No obstante, esta escala permite hacer visible en qué aspectos de la coordinación están las mayores dificultades, lo que hace posible focalizar las intervenciones. En esta línea, las mayores dificultades de la paciente estaban en el control axial, mientras que el control apendicular tenía alteraciones de menor cuantía.
4. Velocidad de marcha en 10 metros: 0.62 m/s. Este valor traduce una limitación moderada de la marcha, con un resultado por debajo del límite que predice una marcha funcional y comunitaria (<1-1,2 m/s)(12). El valor al inicio del período de rehabilitación intrahospitalaria fue de 0,48 m/s. Esto tiene la misma interpretación general, pero se acerca más al límite de 0,4 m/s, bajo el cual la marcha tiende a no ser funcional en un entorno real.
DISCUSIÓN
Las ganglionopatías o neuronopatías sensitivas son un grupo de patologías poco frecuentes. Los reportes de casos en la literatura se centran, principalmente, en el diagnóstico y tratamiento farmacológico precoz, lo que permitiría obtener mejores resultados, ya que se puede evitar un daño neuronal irreversible secundario a la inflamación ganglionar, especialmente en las primeras 8 semanas(5).
Pese a ser una patología discapacitante, la literatura respecto a la rehabilitación en este tipo de neuropatías es escasa(6) y la mayor parte de los estudios se centran en rehabilitación de ataxias cerebelosas(8,13). Cole (1998) reporta un caso de ataxia sensitiva y relata, en términos generales, cómo el favorecer los inputs visuales y sensitivos e incorporar ayudas técnicas y modificaciones permite mejorar la independencia funcional en este tipo de patologías, pero no es riguroso en objetivar los avances y en describir en detalle estas estrategias(6). Por su parte, Chien et al publicaron una revisión narrativa en 2022, en la cual describen las estrategias utilizadas en casos de ataxia. Los autores destacan en este artículo aspectos de la intervención kinesiológica y de terapia ocupacional, el uso de realidad virtual y otras tecnologías y la relevancia de objetivar los avances con instrumentos como el test de balance de Berg o el timed up and go (TUG). Sin embargo, el artículo alude a las ataxias de origen cerebeloso y no a las ataxias sensitivas(13).
Este reporte busca presentar algunas estrategias utilizadas durante el proceso de rehabilitación de esta paciente.
Durante la estadía hospitalaria, se aplicaron diversas estrategias que tienen por finalidad mejorar el input propioceptivo e intervenir sobre los otros sistemas participantes del balance, como el sistema visual. Además, las intervenciones cognitivas permiten generar compensatorias y disminuir el riesgo de lesiones o caídas(6,7).
Si bien la evidencia es limitada, la aplicación de estas estrategias permitió alcanzar un nivel de dependencia moderada al momento del alta, mejorando significativamente en aspectos como el autocuidado y la movilidad. En paralelo, se entrenó a la paciente y familiares en la asistencia adecuada y segura para las actividades de la vida diaria y se coordinó un inicio precoz de la rehabilitación ambulatoria.
El seguimiento de la evolución de los déficits, así como de las limitaciones de la actividad, propios de la evaluación intrahospitalaria, deben realizarse en forma seriada y con escalas específicas. En el caso de las ataxias por ganglionopatía, no existen escalas específicas, lo que exige tener algunas consideraciones. Por ejemplo, la escala SARA evalúa principalmente ataxias de origen central(10). En contraste, en casos de ganglionopatías puede no haber compromiso del habla, lo que dificulta la interpretación del puntaje obtenido.
Respecto a los avances obtenidos, la mejoría funcional sólo pudo objetivarse en forma detallada durante el período de rehabilitación intrahospitalaria intensiva, cuando concurrían todas las estrategias descritas anteriormente. El impacto funcional del tratamiento farmacológico inicial es esperable, ya que se dirige a la etiología del cuadro discapacitante(2), pero la falta de evaluaciones funcionales especializadas en la primera etapa de hospitalización no permitió objetivarlo.
La presentación de este caso cuenta con algunas limitaciones metodológicas que deben considerarse. En primer lugar, la falta de un control no sometido al proceso de rehabilitación descrito no permite observar cómo es la evolución natural de la enfermedad o cómo esta mejora tras el tratamiento farmacológico; sin embargo, el conocimiento de neurociencia clínica y los efectos positivos de la rehabilitación observados en las múltiples enfermedades neurológicas discapacitantes hacen que no sea ético dejar a un paciente sin intervenciones de rehabilitación, ya que constituyen un estándar de cuidado en nuestros tiempos.
Por otro lado, en este caso concurren múltiples intervenciones simultáneamente, haciendo difícil distinguir el impacto particular de cada una de ellas. Para ello se requieren estudios experimentales que permitan controlar variables como la carga terapéutica o la estrategia específica utilizada; sin embargo, la baja incidencia de esta patología complejiza la realización de otros estudios más idóneos para este fin, como un ensayo clínico. Además, frecuentemente, el enorme abanico de desempeño funcional de los pacientes sometidos a rehabilitación, en el cual la severidad y variedad de déficits es muy significativa y no permite homogenizar los casos sólo por el diagnóstico.
Aun considerando estas limitaciones, la evolución favorable del caso descrito releva la importancia de contar con equipos especializados en rehabilitación neurológica, que inicien el seguimiento precozmente —incluso desde las unidades de cuidados críticos o intermedios— y, asimismo, de disponer de opciones de rehabilitación ambulatoria accesibles que aseguren la continuidad de los cuidados. Es este trabajo mancomunado el que permitirá objetivar los avances en el mediano y largo plazo, y abordar otros aspectos relevantes para la rehabilitación, como la participación comunitaria, familiar y laboral.
CONCLUSIÓN
Por la escasa información disponible en la literatura sobre la rehabilitación en ganglionopatías sensitivas, es necesario conocer distintas estrategias que puedan ser de utilidad en la rehabilitación de este tipo de pacientes y para esto es fundamental la participación de los distintos miembros del equipo de rehabilitación. En su mayoría, las estrategias usadas derivan de lo hecho en ataxias cerebelosas, pero con un sustento teórico desde la neurorrehabilitación que sugiere un beneficio potencial. A través de ellas, se obtuvieron resultados favorables en el desempeño funcional de la paciente. Esta brecha de conocimiento plantea la necesidad de generar evidencia y acumular casuística en torno a las estrategias más efectivas para la rehabilitación de pacientes con ganglionopatías sensitivas.
REFERENCIAS
1. Casada V, Morin MA, Añón X, Vuan MF, Rozada R, Sosa L. Ganglionopatía sensitiva. Caso clínico y revisión de la bibliografía. Revista Uruguaya de Medicina Interna 2022:72.
2. Amato AA, Ropper AH. Sensory ganglionopathy. The New England Journal of Medicine 2020;383:1657–62.
3. Tulbă D, Popescu BO, Manole E, Băicuș C. Immune axonal neuropathies associated with systemic autoimmune rheumatic diseases. Front Pharmacol 2021;12:610585.
4. Gwathmey KG. Sensory neuronopathies. Muscle Nerve 2016;53:8-19.
5. Crowell A, Gwathmey KG. Sensory neuronopathies. Curr Neurol Neurosci Rep. 2017;17:79.
6. Cole J. Rehabilitation after sensory neuronopathy syndrome. Journal of the Royal Society of Medicine 1998;91:30–2.
7. Jacobi H, Alfes J, Minnerop M, Konczak J, Klockgether T, Timmann D. Dual task effect on postural control in patients with degenerative cerebellar disorders. Cerebellum & Ataxias 2015;2:6.
8. Zimmet AM, Cowan NJ, Bastian AJ. Patients with cerebellar ataxia do not benefit from limb weights. Cerebellum 2019;18:128.
9. Mishra B, Sudheer P, Agarwal A, Srivastava MVP, Nilima, Vishnu VY. Minimal clinically important difference (MCID) in patientreported outcome measures for neurological conditions: review of concept and methods. Ann Indian Acad Neurol 2023;26:334-43.
10. Berg KO, Wood-Dauphinee SL, Williams JI, Maki B. Measuring balance in the elderly: validation of an instrument. Can J Public Health 1992;83 Suppl 2:S7-11.
11. Kim BR, Lim JH, Lee SA, Park S, Koh SE, Lee IS et al. Usefulness of the scale for the assessment and rating of ataxia (SARA) in ataxic stroke patients. Ann Rehabil Med 2011;35:772-80.
12. Bohannon RW. Comfortable and maximum walking speed of adults aged 20-79 years: reference values and determinants. Age Ageing 1997;26:15-9.
13. Chien HF, Zonta MB, Chen J, Diaferia G, Viana CF, Teive HAG et al. Rehabilitation in patients with cerebellar ataxias. Arq Neuropsiquiatr 2022r;80:306-15.
Correspondencia:
 Dr. Javier Pizarro Soto
Dr. Javier Pizarro Soto
 Unidad de Medicina Física y Rehabilitación, Hospital de San Camilo, San Felipe
Unidad de Medicina Física y Rehabilitación, Hospital de San Camilo, San Felipe
 [email protected]
[email protected]
 569 3525 0321
569 3525 0321